[파이낸셜뉴스] 중국이 개발한 코로나19 백신이 인도네시아에서 해외 첫 대중 접종에 들어간 가운데 효능 논란에 휩싸였다. 학계와 외신들은 백신의 효능이 임상시험마다 천차 만별이라며 중국산 백신의 효능을 의심했다.
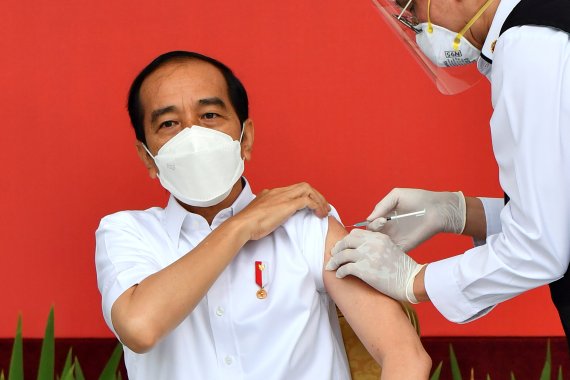
인도네시아 대통령궁은 13일 오전 9시 30분(현지시간)부터 조코 위도도 대통령의 코로나19 백신 접종을 생중계했다. 그가 접종받은 백신은 중국 제약사 시노백 바이오테크가 개발한 '코로나백'이었다.
중국 정부는 지난 7월에 코로나백의 긴급 사용을 허가했으나 아직 광범위한 대중 접종을 시작하지 않았다. 코로나백은 지난 5일 해외에서는 처음으로 볼리비아에서 사용 승인을 얻었다. 그러나 볼리비아는 승인 이후 접종을 미뤘으며 결국 지난 11일 2번째로 사용 승인을 내린 인도네시아가 중국외 국가로는 처음으로 코로나백 대중 접종에 나섰다.
인도네시아는 지난달부터 코로나백을 수입했고 현재 300만회 분량을 확보해 전국 의료시설에 배포했다. 현지 정부는 대통령의 접종을 시작으로 4월까지 현장 의료진과 노인 등에게 백신을 우선 접종하고 4월 이후 내년 3월까지 전체 인구의 70%인 1억8150명에게 백신을 무료 접종할 계획이다.인도네시아는 시노백 백신 외에도 영국 아스트라제네카와 미국 제약사 노바백스, 화이자로부터 각각 5000만회분의 백신을 구입했고 국제 백신 공동구매 기구인 코백스(COVAX)에서도 5400만회 분량의 백신을 받기로 했다.
시노백은 지난해부터 브라질과 터키, 인도네시아에서 3차 임상시험을 진행했다. 인도네시아 당국은 11일 사용 승인에서 코로나백의 면역 효과가 65.3%라고 밝혔다. 세계보건기구가(WHO)가 내놓은 코로나 백신의 최저 효능 기준은 50%다. 이와 관련해 인도네시아 이슬람계 정당인 번영정의당(PKS)의 마르다니 알리 세라 총재는 "시노백 백신의 효과가 65%밖에 안 되는 점은 매우 유감스럽다"며 "효과는 최소 80%는 돼야 한다"고 주장했다. 미 화이자 및 모더나가 개발한 코로나19 백신의 효능은 94~95% 수준이다.
효능 논란은 12일 브라질 정부 연구소의 2차 발표 이후 더욱 증폭됐다. 시노백과 협력해 임상시험을 진행했던 브라질 상파울루 주정부 산하 부탄탕 연구소는 이날 발표에서 1만2500만명을 상대로 진행한 코로나백 3차 임상결과 50.38%의 효능이 나왔다고 전했다. 이는 WHO 기준을 간신히 넘는 숫자다.
부탄탕 연구소는 지난 7일 발표에서 2번의 발표 연기 끝에 코로나백의 효능이 78%라고 주장했다. 현지에서는 첫 발표 이후 시험 과정이 불투명하다는 지적이 쏟아졌고 이에 부탄탕 연구소는 코로나백의 효능이 의료 처치가 필요 없을 정도로 증상이 아주 경미한 환자까지 합하면 50.38%라고 시인했다. 시노백은 지난달 터키 3차 임상에서 1300명 대상 실험 결과 91%의 효능이 나왔다고 주장했으며 인도네시아 임상의 경우 1620명이 참여했다,
미국 비영리 연구기관 사빈백신연구소의 데니스 가레트 연구원은 이날 월스트리트저널(WSJ)을 통해 부탄탕 연구소 발표를 언급하며 "한 번도 본 적 없는 매우 이례적인 상황"이라고 지적했다. 이어 "임상 결과 발표를 두 차례나 미뤘는데 애초 결과가 불만족스러워 보다 유리한 방법을 찾은 것이 아닌가 싶다"고 말했다.
코로나백은 일반적인 백신처럼 2~8도에서 보관이 가능하고 2차례 접종해야 면역 효과를 기대할 수 있다. 중국과 인접한 동남아 국가들은 운송상의 이유로, 남미 및 아프리카 국가들은 가격 때문에 코로나백을 선호하고 있다. 현재 브라질과 칠레, 인도, 인도네시아, 필리핀, 터키, 우르과이 등이 코로나백을 구입한 것으로 알려졌다.
pjw@fnnews.com 박종원 기자
※ 저작권자 ⓒ 파이낸셜뉴스, 무단전재-재배포 금지