관련종목▶
삼성바이오에피스 바이오시밀러 美 진출
SB3도 현재 유럽서 심사중
SK케미칼 혈우병 치료제 '앱스틸라'도 호주 허가
SB3도 현재 유럽서 심사중
SK케미칼 혈우병 치료제 '앱스틸라'도 호주 허가
우리나라 바이오신약과 바이오시밀러(바이오복제약)가 세계시장에서 잇따라 허가를 획득하며 순항하고 있다.
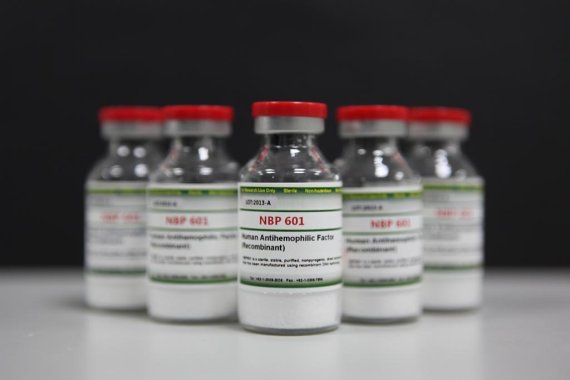
23일 바이오업계에 따르면 SK케미칼은 이날 혈우병 치료제 '앱스틸라(AFSTYLA)'가 호주 식약처(TGA)로부터 최종 시판 허가를 받았다. 이로써 앱스틸라는 국내에서 기술을 개발한 바이오 신약으로는 최초로 미국, 유럽, 캐나다에 이어 호주까지 진출하게 됐다.
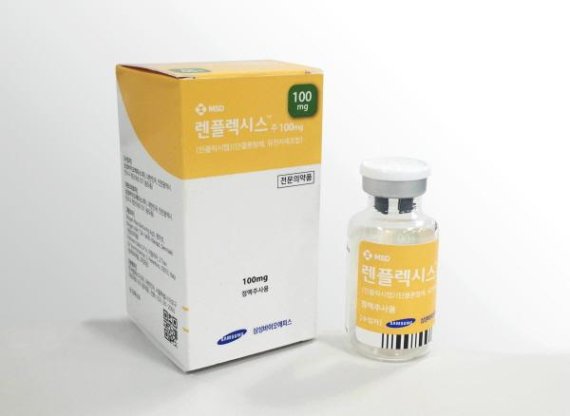
삼성바이오에피스는 지난 21일 미국 식품의약국(FDA)로부터 자가면역질환 치료제인 렌플렉시스(SB2, 성분명 인플릭시맙)에 대한 판매 허가 승인을 받았다. 이번 승인은 한국(2015년), 유럽, 호주(이상 2016년)에 이어 렌플렉시스(유럽명 플릭사비)의 네번째 판매 허가 승인이다.
■美 바이오시밀러 시장 확대
삼성바이오에피스가 허가받은 렌플렉시스는 2016년 기준 전세계에서 연간 9조3000억원 이상 팔리는 존슨앤존슨의 항체의약품인 '레미케이드'의 바이오시밀러다. 이 약은 류머티스 관절염, 궤양성 대장염, 크론병, 강직성 척추염, 건선성 관절염 및 건선에 적응증을 가지고 있다. 삼성바이오에피스는 연구개발(R&D) 역량 및 제품이 국제적으로 인정받는 계기가 됨은 물론 삼성의 바이오시밀러가 세계 최대 바이오 의약품 시장인 미국에서 글로벌 제약사들과 당당히 경쟁할 수 있는 초석을 마련한 셈이라고 분석했다.
삼성바이오에피스는 지난해 3월 미국 FDA에 렌플렉시스 판매 허가 신청을 하고 13개월만에 허가 승인을 받았으며 파트너사인 글로벌 제약사 머크사가 미국에서의 판매를 담당할 예정이다.
삼성바이오에피스 고한승 사장은 "이번 미국 판매 허가 승인은 회사 창립 5년만에 이룬 쾌거이며 유럽에 이어 미국에서도 더 많은 자가면역 질환 환자들이 바이오의약품으로 치료 받을 기회를 가질 수 있을 것으로 기대된다"며 "현재 진행 중인 바이오시밀러의 매출 확대에 더욱 박차를 가할 것"이라고 말했다.
삼성바이오에피스는 현재 엔브렐 바이오시밀러(SB4, 성분명 에타너셉트)인 브렌시스를 호주, 캐나다, 한국, 유럽(유럽명 베네팔리)등에 판매 중에 있다. 또 휴미라 바이오시밀러(SB5, 성분명 아달리무맙), 허셉틴 바이오시밀러(SB3, 성분명 트라스투주맙)는 유럽의약품청(EMA)에서 판매 허가 심사 중에 있다.
한국투자증권 정보라 애널리스트는 "미국은 유럽과 달리 자국 의약산업을 보호한다는 명목으로 바이오시밀러 시장 도입에 다소 소극적인 입장을 보이고 있었다"며 "하지만 트럼프 행정부 역시 시장 경쟁 유도를 통해 약가를 인하하겠다는 입장이기 때문에 바이오시밀러 시장 진입이 유리한 상황이고 2016년 셀트리온의 렘시마를 시작으로 바이오시밀러 허가가 늘어나고 있어 미국 바이오시밀러 시장 점유율 확대 전망은 긍정적인 상황"이라고 분석했다.
■앱스틸라, 호주서도 허가
SK케미칼이 개발한 앱스틸라는 지난 2009년 CSL에 기술 수출된 후 CSL사에서 생산 및 글로벌 임상, 허가 신청을 진행해왔다.
앱스틸라는 지난해 5월 FDA의 시판 허가를 받아 국내 바이오 신약 중 최초로 미국 내 판매에 돌입했고 12월 캐나다, 지난 1월 유럽에서도 시판 허가를 획득했다. 또 스위스, 일본 등에서 허가 심사 단계에 있다. 앱스틸라는 SK케미칼이 세계에서 최초로 연구 개발한 '단일 사슬형 분자구조(single-chain product)'를 가진 혈액응고 제8인자이다. 기존 혈우병치료제는 분리된 두 개의 단백질이 연합된 형태였지만 앱스틸라는 두 단백질을 하나로 완전 결합시켜 안정성을 획기적으로 개선했으며 주 2회 복용으로도 지속적인 출혈 관리 효과를 볼 수 있다.
CSL은 앱스틸라가 전세계 A형 혈우병치료제 시장에서 혁신적인 치료제로서 자리매김할 것으로 예상하고 있으며 이에 따라 SK케미칼은 글로벌 판매에 따른 로열티와 판매 마일스톤을 기대하고 있다.
CSL의 R&D 총괄 관리자 앤드류 커버슨 박사는 "앱스틸라의 호주 시판 허가를 통해 환자들이 보다 나은 삶을 위한 치료 대안을 얻게 됐다"고 말했다.
SK케미칼 박만훈 사장은 "백신.혈액제 등 바이오 사업에 대한 오랜 투자를 통해 일궈낸 성과들이 글로벌에서 역량을 인증받고 있다"며 "국내를 넘어 세계 인류의 건강을 증진시키기 위한 투자를 지속할 것"이라고 말했다.
세계혈우병재단에 2015년 조사한 보고서에 따르면 호주에선 연간 1억 4600만 IU(International Unit)의 제8인자 결핍 A형 혈우병치료제가 처방되고 있고 이중 95%가 앱스틸라와 같은 유전자재조합 제품이다. 유전자재조합 제8인자 혈우병치료제의 경우 현재 10 IU당 평균 3~6 AUD(호주달러) 정도의 가격을 형성하고 있다.
글로벌리서치업체 데이터모니터에 따르면 A형 혈우병 치료제 전 세계 시장은 연 8조2000억원(72억 달러)에 달한다. 관련 시장은 지속적으로 성장하고 있으며 2020년에는 전 세계 시장이 약 17% 증가한 9조5000억원(83억 달러)에 이를 것으로 예상되고 있다.
pompom@fnnews.com 정명진 의학전문기자
※ 저작권자 ⓒ 파이낸셜뉴스, 무단전재-재배포 금지