중국의 발암물질 혈압약 원료 소동은 전세계 제약산업의 공급망이 위험에 그대로 노출돼 있음을 드러내는 것이라고 파이낸셜타임스(FT)가 6일(현지시간) 보도했다.
전문가들은 제약업계의 비용절감 노력과 이에따른 세계화가 결국은 규제완화를 부른 셈이라면서 당분간은 상황이 크게 개선되기 어려울 것으로 비관했다. 다만 중국이 바이오산업을 차세대 산업으로 육성하려는 목표를 갖고 있어 제약 관련 규정과 감독 강화가 중장기적으로는 품질 개선으로 이어질 것으로 예상했다.
■ 中, 전세계 생약원료 40% 담당
중국산 혈압약 원료에서 발암물질이 검출됐다는 소식은 전세계를 뒤흔들고, 중국의 제약산업 규제와 감독이 얼마나 소홀한 지, 또 이 같은 중국의 느슨한 감독이 전세계 제약 소비자들의 안전을 얼마나 좌우할 수 있는지를 분명하게 보여줬다.
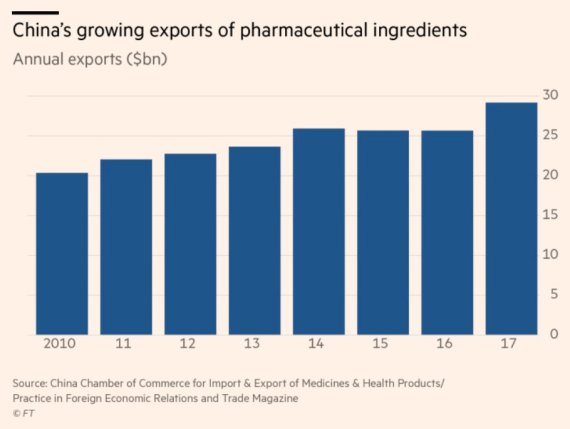
중국은 세계 최대 생약원료(API) 생산국으로 영국 의약건강제품감독국(MHRA)에 따르면 전세계 API의 40%를 생산한다.
중국 당국 통계에 따르면 지난해 중국이 수출한 생약원료는 290억달러어치로 테바제약을 비롯한 복제약 제조업체들, 존슨앤드존슨(J&J), 노바티스 같은 다국적 제약업체들이 이를 수입했다.미국의 경우 생약원료 80%가 중국과 인도에서 수입된다.
그러나 중국의 감독은 허술하다. 회계.컨설팅업체 언스트앤드영(EY) 중국의 존 린 파트너는 “상당수 중국 API 업체들이 기존 제조공정을 엄격히 지키지 않고 있고, 기록도 엄격히 보관하지 않는다”면서 “(중국을 포함한 각국) 감독당국이 직원 부족을 이유로 API 업체들에 대한 현장조사를 게을리하고 있다”고 지적했다.
특히 중국의 의약품 관리 규정은 내수용 없이 수출만 하는 API 업체들에 대해서는 중국 당국이 조사를 하지 않아도 되도록 하고 있다. 수출 생약원료 품질 검사는 수입업체가 직접 해 정기적으로 미 식품의약품안전청(FDA), 유럽의약청(EMA) 등 감독당국에 제출토록 돼 있다.
■ 중국산 원료 각국 경고도 급증
세계 각국의 중국 생약원료에 대한 경고는 급증하고 있다. FDA가 중국 제약원료 업체들에 경고한 사례는 2014년 5건에서 지난해 22건으로 껑충 뛰었다. FDA가 보내는 경고서한은 중국 업체들을 벌벌 떨게 한다. FDA 베이징사무소 책임자는 중국 업체들에 ‘저승사자(the killer)’로 통한다. FDA는 올들어 11건, EMA는 6건의 경고서한을 보냈다. EMA의 경우 매년 중국 API 업체 20~40 곳에 대한 현장 조사를 실시하고, 이가운데 약 10%에서 규정 위반을 적발해내고 있다.
의료부문 싱크탱크인 더헤이스팅스센터의 로즈매리 깁슨은 품질 저하의 진짜 원인은 제약업계의 비용절감에 있다면서 “(비용절감을 위한) 세계화가 사실상의 규제완화 효과를 내고 있다”고 비판했다.
한편 중장기적으로는 중국 제약산업의 품질 역시 개선될 것으로 예상됐다. 자국민 안전을 위한 노력과 함께 중국이 바이오부문을 세계적인 수준으로 육성하고, 지금처럼 생약원료가 아닌 완성약 수출을 확대한다는 목표를 갖고 있기 때문이다. 그러나 단기간에 개선을 기대하기는 어렵다는 비관 역시 만만찮다. 지방정부가 여전히 중소업체 보호에 급급한 데다 규제 당국 공무원들이 박봉으로 뇌물에 취약하기 때문에 적어도 몇 년은 지나야 규제가 정착되고, 안전기준 역시 따라서 올라갈 것으로 이들은 예상했다.
dympna@fnnews.com 송경재 기자
※ 저작권자 ⓒ 파이낸셜뉴스, 무단전재-재배포 금지