관련종목▶
기존치료제 한계점 극복…생산공정이 간단해 생산효율성·비용면에서 ↑
‘NK cell engager 치료제’ 공동개발 임상 비용 공동부담, 향후 특허권 공동 소유
‘NK cell engager 치료제’ 공동개발 임상 비용 공동부담, 향후 특허권 공동 소유
[파이낸셜뉴스] 코스닥 상장사 엔케이맥스는 미국 자회사를 통해 아피메드(Affimed NV, NASDAQ: AFMD)와 CAR-NK를 대체할 ‘EGFR 표적형 NK세포치료제’ 공동개발 계약을 체결했다고 21일 밝혔다.
양사는 이번 계약을 통해, EGFR 양성 고형암 환자를 대상으로 하는 ‘슈퍼NK’-‘AFM24(CD16A/EGFR 표적형 ICE)’ 결합 치료제 개발을 위한 미국 임상1/2a상 pre-IND 미팅을 곧 진행할 계획이다. 해당 임상 비용은 양사가 공동 부담하며, 향후 특허권은 양사가 공동 소유하게 된다. 비소세포폐암, 두경부종양, 대장암, 췌장암, 유방암 등이 대표적인 EGFR 양성 암종이다.
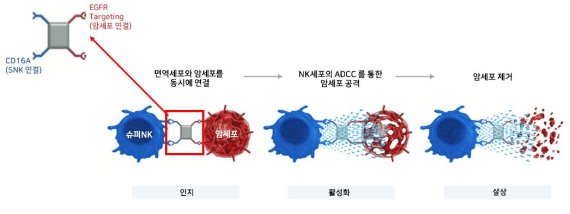
아피메드의 표적형 Innate Cell Engager(ICE) ‘AFM24’는 EGFR 발현 암세포와 선천면역세포인 NK세포의 CD16A 수용체를 연결하는 매개체로, NK세포의 ADCC(Antibody Dependent Cellular Cytotoxicity, 항체 의존성 세포독성) 및 ADCP(Antibody-Dependent Cellular Phagocytosis, 항체 의존성 세포포식작용)을 통해 암살상효과를 유도한다. 앞서 2018년도에는 로슈(Roche)의 계열사인 제넨텍(Genentech)이 관련 플랫폼 기술을 5.5조원 규모로 기술이전(License In) 받은 바 있다. 이 외에도 아피메드는 머크, MD앤더슨, 다케다 등 유수의 글로벌 제약사들과 공동임상을 진행 중이다.
아피메드의 아디 호에스(Adi Hoess) CEO는 “연구 결과 NK세포의 숫자는 암환자 치료와 관련이 높다는 것을 확인했다”며 “AFM24와 슈퍼NK가 결합함으로써 사망률이 높은 EGFR 양성 고형암 환자들에게 임상적으로 의미 있는 치료 대안을 제공할 수 있을 것이다. 또한, AFM24는 CD16A 결합도가 높아 슈퍼NK와 강력하게 결합해 EGFR 발현율이 낮은 암환자에게도 치료효과가 높을 것이라 기대한다”고 말했다.
그러면서“이번 공동개발 이외에도 슈퍼NK와 자사의 표적형 ICE 플랫폼 기술을 결합하는 파이프라인 확장도 고려 중이다”고 전했다.
엔케이맥스 김용만 연구소장은 “암환자들의 경우 NK세포 활성도가 낮아 ICE와 NK세포의 결합이 어렵고, 치료효과도 높지 않았다. 이에 아피메드는 공동임상을 진행할 고활성의 NK세포치료제를 찾던 중, CD16A, NKG2D, NKp30, NKp46 등 NK세포 활성화 수용체의 발현도가 높고 암세포 살상능력을 80배 이상 향상시킨 슈퍼NK와 AFM24를 결합하는 이번 계약을 체결하게 됐다”며, “지난 6월 양사가 물질이전계약(Material Transfer Agreement, MTA)을 맺고 실험(In-vitro test)한 결과 AFM24와 자가 및 동종 슈퍼NK 모두 결합도가 우수하고, NK세포를 효율적으로 활성화시킬 뿐만 아니라 암살상효과도 크게 증가하는 것을 확인했다”고 덧붙였다.
엔케이맥스 아메리카의 폴 송(Paul Y. Song) 부사장은 “고활성 슈퍼NK에 아피메드의 ICE를 접목할 경우, CAR-NK처럼 암세포를 정확하게 추적해 공격할 수 있다”며 “또한, 이는 생산공정이 복잡한 CAR-NK/CAR-T보다 결합이 단순해 생산효율성 향상 및 비용 절감 효과가 있을 뿐 아니라 림프구 제거술(lymphodepletion)도 필요하지 않아 향후 CAR-NK를 대체할 수 있는 기술이 될 것이다”고 설명했다.
그는 이어, “AFM24와 자가 및 동종 슈퍼NK 결합은 CAR-NK의 복잡한 엔지니어링 과정과 항체치료제의 부작용 등 기존 치료제가 가진 한계점을 극복하여 항암제의 새로운 패러다임을 제시할 것이라 생각한다”며 “이는 글로벌제약사의 고활성 NK세포치료제 슈퍼NK 수요 증가로 이어져 기술이전 논의 또한 활발해질 것”이라고 언급했다.
kakim@fnnews.com 김경아 기자
※ 저작권자 ⓒ 파이낸셜뉴스, 무단전재-재배포 금지